用于活性氧清除抗炎治疗的设计师纳米酶
在最近的一份报告中,Yufeng Liu 和的一个跨学科研究团队开发了一种集成的纳米酶级联,以消除过多的活性氧(ROS;氧自由基)。纳米酶模仿超氧化物歧化酶(一组酶)并结合基于锰 (Mn) 的金属有机框架(MOF) 将氧自由基转化为过氧化氢 (H 2 O 2 )。使用实验室和体内实验,该团队展示了集成级联纳米酶的 ROS 清除潜力。作为概念证明,他们缓解了两种形式的炎症性肠病(IBD)——使用级联纳米酶作为有效治疗的溃疡性结肠炎和克罗恩病。该研究提供了一种构建酶样级联系统的新方法,并说明了它们在体内治疗 IBD 的有效疗法的前景。这项工作现在发表在Science Advances 上。
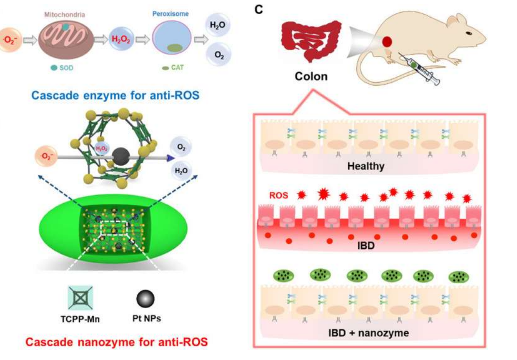
在生物体内发生的级联催化反应中,多种酶在亚细胞区室内结合,以实现准确的信号转导和有效的代谢。与传统的多步反应相比,这种受限的级联反应是有利的,因为扩散势垒降低和中间体的局部浓度提高,从而提高了原子经济性和总体反应。科学家们已经做出了大量努力来模拟这种级联系统在支架上,但它们的高成本和低稳定性限制了广泛的实际应用。因此,研究人员探索了酶模拟物,以在实验室中理解和构建级联反应。在这项工作中,刘 e al。详细介绍了一种具有高活性的基于单组分纳米酶的级联反应系统,并证明了它们在活性氧 (ROS) 相关炎症性肠病 (IBD) 的体内治疗中的作用。
酶支架的设计、合成和表征
该团队设计并合成了一种集成的超氧化物歧化酶 (SOD) 和过氧化氢酶(CAT) 模拟级联纳米酶,并将其命名为 Pt@PCN222-Mn。为了构建支架,他们在名为 PCN222的纳米级锆 (Zr)基金属有机框架(MOF) 中引入了类似 SOD 的锰 (Mn) (III) 卟啉部分和类似 CAT 的铂纳米颗粒。集成构建体(Pt@PCN222-Mn)显示出增强的 ROS 清除活性,以保护小鼠免受 ROS 相关 IBD(一种迄今无法治愈的慢性疾病)的侵害,从而扩大级联纳米酶在体内生物医学应用中的潜力。
在实验过程中,刘等人。使用核磁共振、傅里叶变换红外光谱和紫外可见光谱测量证实了初步锰基结构的成功合成。该团队合成了包含纳米级 MOF 的组件,并用透射电子显微镜(TEM) 和扫描电子显微镜(SEM)确认了其形成。然后,科学家们开发了三种级联纳米酶,并将它们分别命名为 Pt@PCN222-Mn-1、Pt@PCN222-Mn-3 和 Pt@PCN222-Mn-5。其中,与迄今为止研究的其他抗 ROS 纳米酶相比,Pt@PCN222-Mn-5 具有更高的表面积。
研究级联纳米酶的催化活性
Pt@PCN222-Mn-3 和 Pt@PCN222-Mn 存在下,H2O2 (50 mM) 分解产生氧气的典型动力学曲线-5. (D) 前 60 秒的产氧速度与纳米酶浓度之间的依赖性。数据显示为平均值 ± SD (n = 3)。图片来源:科学进展,doi:10.1126/sciadv.abb2695
作为生物环境中 ROS 清除级联反应的第二个关键步骤,CAT(过氧化氢酶)酶催化过氧化氢 (H 2 O 2 ) 分解为水和氧气。刘等人。因此,通过监测分解过氧化氢产生的氧气来监测纳米酶的类 CAT 活性。和以前一样,Pt@PCN222-Mn-5 在基于 MOF 的酶模拟物中表现出最高的 CAT 样活性。根据结果,刘等人。证实 SOD 样活性是由酶构建体的锰结合部分引起的,而整体铂纳米颗粒主要负责 CAT 样活性。
聚焦酶Pt@PCN222-Mn-5与体内抗炎治疗
为了充分理解级联纳米酶 Pt@PCN222-Mn-5 的活性,该团队研究了其协同 SOD 样和 CAT 样酶活性,并观察到后者的显着协同效应。该团队选择纳米酶进行进一步研究,并在细胞毒性研究期间用细胞系测试其功能。在低于 80 µg/mL 的浓度下,纳米酶没有表现出任何细胞毒性,并表现出出色的活性氧扫描潜力。
根据实验结果,Liu 等人。在该疾病的小鼠模型中进行了体内治疗以治疗溃疡性结肠炎 (UC) 和克罗恩病 (CD)。由于 UC 是一种炎症性肠病,通常伴有由于活性氧过量产生,科学家们测试了 Pt@PCN222-Mn-5 与现有 IBD 治疗药物的治疗效果。该团队通过腹腔注射对每只小鼠进行治疗,并观察到 Pt@PCN222-Mn-5 对缓解小鼠 UC 疾病状态的成功治疗效果。该团队使用几个治疗组优化了级联纳米酶的剂量,发现感兴趣的焦点酶是最有利的。当他们类似地使用疾病诱导的小鼠模型探索 CD,另一种类型的 IBD 时,治疗策略表明与 IBD 治疗中使用的传统小分子药物相比,级联纳米酶的疗效更高。
通过这种方式,Yufeng Liu 及其同事开发了一种集成纳米酶来催化级联反应并消除活性氧 (ROS)。集成的纳米酶具有两个空间分离的活性位点,以模拟超氧化物歧化酶 (SOD) 和过氧化氢酶 (CAT)。通过实验室实验,他们展示了级联纳米酶出色的 ROS 清除活性、优异的生物相容性和良好的水分散性。该团队建立了炎症动物模型,以测试级联纳米酶在生物有机体中的抗 ROS 能力,并确定它们对溃疡性结肠炎(UC) 和克罗恩病 (CD) 炎症性肠病 (IBD) 模型的优越治疗潜力。该团队优化了纳米酶的浓度在动物模型中实现IBD的有效缓解。该工作显示出用于炎症治疗的优异 ROS 清除活性,并为构建具有多个活性位点的纳米酶在生物医学中的进一步应用提供了一种有前景的方法。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
大众CC作为一款备受关注的中型轿车,凭借其优雅的设计和出色的性能一直吸引着众多消费者的目光。2025款大众CC...浏览全文>>
-
2025款阜阳途锐新车正式上市,凭借其卓越的性能和豪华配置吸引了众多消费者的关注。这款车型以最低售价55 88...浏览全文>>
-
在准备购买一辆汽车之前,了解车辆的落地价格是非常重要的。所谓落地价,是指购车时除了车款之外还需要支付的...浏览全文>>
-
安徽淮南地区的长安启源E07作为一款备受关注的新能源车型,凭借其时尚的设计、丰富的配置以及出色的续航能力,...浏览全文>>
-
安徽淮南长安启源A05 2025款新车现已正式上市,这款车型以其高性价比和出色性能吸引了众多消费者的关注。作为...浏览全文>>
-
安徽阜阳地区的威然车型在近期进行了配置上的升级,对于想要购买这款MPV的消费者来说,这是一个值得关注的消息...浏览全文>>
-
随着汽车市场的不断发展,SUV车型因其宽敞的空间和多功能性受到了越来越多消费者的青睐。作为大众旗下的高端旗...浏览全文>>
-
安徽蚌埠地区想要购买长安启源E07这款新能源汽车的朋友,可以参考以下信息来做出更明智的选择。长安启源E07定...浏览全文>>
-
随着汽车市场的不断发展,2025款安庆高尔夫作为一款备受关注的车型,其价格和配置自然成为消费者热议的话题。...浏览全文>>
-
近期,安徽蚌埠地区的帕萨特车型迎来了新一轮的价格调整,其落地价再次创下新低,吸引了众多消费者的关注。作...浏览全文>>
- 悉尼最后几个年薪低于 10 万美元的郊区
- 2025 年新南威尔士州值得投资的地方
- 揭秘在澳大利亚买房需要多少收入
- 悉尼最后几个年薪低于 10 万美元的郊区
- 昆士兰有望成为澳大利亚房地产强国之一
- MSI 推出首款双模式 4K 曲面电竞显示器
- 飞利浦 Screeneo GamePix 900:在发布前进行预览
- 您会在这个奇怪的电动露营三轮车里露营吗
- Meross 推出支持 Matter 的智能恒温器
- 配备出色 3K OLED 显示屏的 Acer Swift 16 现已降价至史上最低价
- Acer Predator Helios 18 RTX 4080 游戏笔记本电脑 现优惠 725 美元
- VivoX200Pro视频和新样张揭示了200MP蔡司变焦相机的锐利眼睛可以达到多远
- 派对氛围天文爱好者又一次欣赏到极光秀
- iPhone16相机控制按钮有史以来最不苹果的东西
- 贾雷尔夸萨与利物浦签订新合同
- 首款在安兔兔上得分300万的手机拥有非常强大的SoC即将发布
- HumaninMotionRobotics的自平衡XoMotion外骨骼获得加拿大批准用于物理治疗
- 龙宫样本对之前关于富碳小行星形成的观点提出了质疑
- 凯文德布劳内伤情更新曼城球星的伤势进展和可能的回归日期
- 实验室实验表明用核武器轰炸一颗巨大的小行星可以拯救地球
